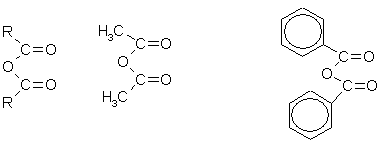Одноосновные карбоновые кислоты химические свойства. Высшие карбоновые кислоты. Номенклатура и изомерия
Классификация
Органические карбоновые кислоты характеризуются наличием карбоксильной группы –СООН . Карбоновые кислоты классифицируют по числу карбоксильных групп и по строению углеводородного радикала. В зависимости от числа карбоксильных групп кислоты делят на одно-, двух, трех и многоосновные. В зависимости от строения углеводородного радикала кислоты делят на предельные, непредельные и ароматические. Радикалы, входящие в состав кислот, могут быть циклические и ациклические.
Предельные одноосновные кислоты
Одноосновные предельные карбоновые кислоты образуют гомологический ряд с общей формулой С n H 2n O 2 (n = 1,2,3...) или C n H 2n+1 COOH (n = 0,1,2...). Изомерия предельных одноосновных карбоновых кислот обусловлена только изомерией углеводородного радикала. Формулы и названия некоторых кислот приведены в таблице:
Предельные карбоновые кислоты |
ФОРМУЛА | Название |
| Тривиальное | по ИЮПАК | |
| муравьиная | метановая | |
 | уксусная | этановая |
 | пропионовая | пропановая |
 | масляная | бутановая |
 | изомасляная, диметилуксусная | бутановая |
 | валериановая | пентановая |
 | изовалериановая | 3-метилбутановая |
 | триметилуксусная | 2,2-диметилпропановая |
Физические свойства
Низшие кислоты (муравьиная, уксусная, пропионовая) – бесцветные остропахнущие жидкости, кислоты с числом атомов углерода от 4 до 9 – маслянистые жидкости с неприятным запахом, с числом атомов углерода больше 10 – твердые вещества. Растворимость кислот в воде резко уменьшается по мере увеличения числа атомов углерода в молекуле. Температуры кипения кислот возрастают по мере увеличения молекулярной массы, при этом температуры кипения кислот, содержащих одинаковое число атомов углерода и имеющих неразветвленный радикал, выше, чем у кислот с разветвленным радикалом. Кислоты кипят при значительно более высоких температурах, чем соответствующие им спирты. Это связано со значительно большей ассоциацией молекул кислот.
Химические свойства
Реакции кислот, обусловленные карбоксильной группойПерераспределение электронной плотности в карбоксильной группе показано на рисунке:

В результате полярность связи О-Н настолько велика, что сравнительно легко протекает диссоциация кислоты:

Образующийся анион обладает повышенной стабильностью за счет резонанса:

Сила карбоновых кислот зависит от радикала, связанного с карбоксильной группой и определяется величиной положительного заряда на карбоксильном углероде. С увеличением этого заряда сила кислоты возрастает, с уменьшением – убывает. В свою очередь, величина этого заряда определяется знаками эффектов (индуктивного и мезомерного), действующих со стороны радикала. Так как положительный индуктивный эффект углеводородного радикала увеличивается с увеличением числа атомов углерода и с увеличением разветвленности радикала, сила соответствующих карбоновых кислот убывает. Муравьиная кислота относится к кислотам средней силы, все остальные одноосновные предельные кислоты – слабые. Растворимые в воде кислоты создают в растворе кислую среду, достаточную для изменения окраски индикаторов.
1. Карбоновые кислоты взаимодействуют с металлами, оксидами и гидроксидами металлов, образуя соли:
2CH 3 COOH + Zn = (CH 3 COO) 2 Zn + H 2 2CH 3 COOH + CaO = (CH 3 COO) 2 Ca + H 2 O CH 3 COOH + NaOH = CH 3 COONa + H 2 OКарбоновые кислоты сильнее угольной кислоты, поэтому они способны разлагать карбонаты:
CH 3 COOH + Na 2 CO 3 = CH 3 COONa + CO 2 + H 2 O2. При действии на карбоновые кислоты галогенидов фосфора или хлористого тионила гидроксил карбоксильной группы замещается на галоген и образуются галогенангидриды кислот:
3. Со спиртами карбоновые кислоты вступают в реакцию этерификации , в результате которой образуются сложные эфиры. Реакция протекает обратимо в кислой среде. Катализатором этерификации служат минеральные кислоты, например, серная. На первой стадии реакции протонируется кислород карбоксильной группы:

Затем образовавшийся катион подвергается нуклеофильной атаке молекулой спирта:

Промежуточный комплекс может обратимо терять молекулу воды и протон, превращаясь в результате в сложный эфир:

В щелочной среде сложный эфир необратимо гидролизуется с образованием спирта и соли исходной кислоты. Эта реакция называется омылением сложного эфира.
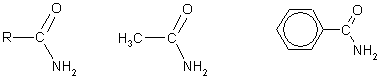
4. Карбоновые кислоты образуют функциональные производные , к которым относятся галогенангидриды, сложные эфиры, ангидриды, амиды и нитрилы кислот. Ангидриды, амиды и нитрилы непосредственно из кислот чаще всего получить невозможно, поэтому используют косвенные методы.
Ангидриды кислот получают нагреванием галогенангидрида и натриевой соли кислоты, например:

Амиды образуются при обработке галогенангидридов кислот аммиаком:

при сухой перегонке (нагревании) аммониевых солей карбоновых кислот:

или при неполном гидролизе нитрилов кислот:

Нитрилы получаются в результате нуклеофильного замещения атома галогена цианогруппой:
или при обезвоживании амида кислоты оксидом фосфора (V) при нагревании:

Большинство реакций с участием функциональных производных карбоновых кислот протекает по механизму нуклеофильного замещения S N 1 и S N 2, в котором функциональные производные являются субстратами. Например, в разбавленных водных растворах гидролиз хлорангидридов кислот проходит преимущественно по механизму S N 1, на первой, самой медленной стадии которого (именно эта стадия и определяет скорость всего процесса) происходит диссоциация исходного хлорангидрида:

На второй стадии следует быстрая нуклеофильная атака молекулы воды на карбоксильный углерод, и после ухода протона образуется конечный продукт гидролиза - карбоновая кислота:
При бимолекулярном замещении S N 2 нуклеофильная атака и уход иона хлора происходят одновременно:
Бимолекулярный механизм преобладает при низком содержании воды в реакционной системе. Ниже приведены некоторые реакции нуклеофильного замещения в функциональных производных кислот.
Галогенангидриды кислот разлагаются водой (гидролиз):
реагируют со спиртами с образованием сложных эфиров (алкоголиз):
Сложные эфиры получаются и при взаимодействии галогенангидридов с алкоголятами:
В результате взаимодействия галогенангидридов с солями карбоновых кислот образуются ангидриды, таким путем можно получить и смешанные ангидриды, содержащие остатки разных кислот:
При действии на галогенангидриды кислот аммиака (аммонолиз) образуются амиды:
Под действием пероксидов галогенангидриды кислот образуют перекиси ацилов:
Ангидриды кислот при нагревании с водой гидролизуются:

подвергаются алкоголизу при нагревании со спиртом, при этом образуется сложный эфир и кислота:

Под действием аммиака происходит аммонолиз ангидрида, в результате получается амид и соль кислоты:

Амиды кислот гидролизуются при кипячении с водными растворами кислот и щелочей:

Атом водорода в аминогруппе амида может замещаться металлом, например:
Получение кислот
Кислоты можно получить следующими способами:
1. Окислением первичных спиртов, например:

2. Окислением альдегидов различными окислителями, такими, как хромовая смесь, перманганат калия, гидроксид диамминсеребра, кислород - в схеме реакции окислитель показан как [O]:

3. Гидролизом ангидридов, галогенангидридов и нитрилов кислот.
4. С помощью металлорганических соединений, например:

5. С помощью магнийорганических соединений:

Особенности свойств муравьиной кислоты
Муравьиная кислота проявляет свойства альдегида и кислоты, т.к. содержит как карбоксильную группу (обведена синим цветом), так и альдегидную (обведена красным):

Муравьиная кислота - хороший восстановитель:
HCOOH + OH Ag + CO 2 + H 2 O - реакция серебряного зеркала HCOOH + HgCl 2 Hg + CO 2 + 2HClПри нагревании с концентрированной серной кислотой муравьиная кислота дегидратируется с образованием СО:

Муравьиная кислота образует ортоэфиры - сложные эфиры нестабильной ортоформы кислоты:
Этиловый эфир ортрумуравьиной кислоты называется ортомуравьиный эфир :
Получают ортомуравьиный эфир кипячением этилата натрия с хлороформом по реакции:
Сложноэфирная конденсация
Сложноэфирная конденсация (по Кляйзену) протекает при действии алкоголятов щелочных металлов на сложные эфиры карбоновых кислот. Алкоголят-анионы, образующиеся в результате диссоциации:
отрывают протоны из -положения кислотного радикала сложного эфира:

Образовавшийся анион нуклеофильно атакует карбоксильный атом углерода другой молекулы сложного эфира:

Образовавшийся анион отщепляет алкоголят-ион и переходит в продукт конденсации:

который представляет собой сложный эфир (в данном примере - этиловый) 3-оксокислоты. Таким способом из этилацетата можно получить ацетоуксусный эфир (этиловый эфир 3-оксобутановой кислоты). В подобных условиях протекает конденсация сложных эфиров и кетонов, в которой кетон выступает в качестве метилекновой компоненты, а сложный эфир - в качестве карбонильной. При конденсации по-Кляйзену этилацетата и ацетона образуется ацетилацетон - пентандион-2,4.
Органические соединения, называемые карбоновыми кислотами, - класс органических соединений, в составе молекул которых содержатся карбоксильные группы, -COOH, одна или несколько. Лёгкое отщепление протона карбоксильной группы обуславливает кислые свойства таких соединений.
Номенклатура и строение органических соединений
Название в номенклатуре ИЮПАК строится из названия углеводорода, соответствующего углеродной цепочке, содержащей функциональную группу, с окончанием «овая » и добавлением слова «кислота ». Атом углерода в составе карбоксильной группы считается первым в углеводородной цепочке. Например, для формулы СН3-СН2-COOH название вещества - пропановая кислота, а СН3-С(СН3)-СООН - 2-метилпропановая, CH3CH2CH2COOH - бутановая.
Рациональная номенклатура к названию углеводорода требует добавления окончания «карбоновая » и слова «кислота », причём атом углерода карбоксила в нумерацию не включается. Например, этилкарбоновая кислота - СН3-СН2-СООН.
 У многих веществ гомологического ряда кислот есть тривиальные названия
. Например, уксусная (СН3-СООН), муравьиная (НСООН), валериановая (С4Н8-СООН), маргариновая (С16Н33-СООН) и многие другие.
У многих веществ гомологического ряда кислот есть тривиальные названия
. Например, уксусная (СН3-СООН), муравьиная (НСООН), валериановая (С4Н8-СООН), маргариновая (С16Н33-СООН) и многие другие.
Функциональная группа COOH состоит из карбонила - CO и гидроксила - OH, тем не менее свойства кислот отличаются от свойств альдегидов и спиртов, содержащих в своём составе эти группы.
Общая формула предельных одноосновных карбоновых кислот^ R-COOH, где R - углеводородный радикал.
Классификация карбоновых кислот
В зависимости от того, с каким радикалом связан карбоксил, кислоты разделяют на следующие:
- ареновые;
- алифатические;
- алициклические;
- гетероциклические.
По насыщенности углеводородного радикала разделяют насыщенные (предельные, алкановые) и ненасыщенные (непредельные).
При других функциональных группах кислоты будут называться гетерофункциональными, например, аминокислоты, нитрокислоты и т. д.
Качественные реакции
Самые основные качественные реакции органической химии:
- окраска индикатора - красное окрашивание лакмуса;
- реакция с карбонатами или гидрокарбонатами, например, с содой - выделение СО2;
- реакция этерификации - характерный запах продукта реакции (эфира).
Физические свойства
С увеличением массы молекулы уменьшается плотность и растворимость в воде , температура кипения же, напротив, увеличивается. Так, низшие, например, уксусная и муравьиная кислоты являются растворимыми в воде жидкостями, а высшие карбоновые кислоты, такие как пеларгоновая, стеариновая, пальмитиновая и другие - твёрдые вещества, которые в воде не растворяются.
 Молекулы монокарбоновых кислот образуют довольно прочные водородные связи. В твёрдом и жидком состояниях они находятся в виде циклических димеров, а в водных растворах - в виде линейных.
Молекулы монокарбоновых кислот образуют довольно прочные водородные связи. В твёрдом и жидком состояниях они находятся в виде циклических димеров, а в водных растворах - в виде линейных.
Интересная закономерность наблюдается в изменении температур плавления кислот нормального строения. Кислоты, количество атомов углерода в радикале, которых чётное, кипят при более высоких температурах, чем имеющие нечётное. Объясняется это симметричностью строения молекул с чётным количеством углеродных атомов и, как следствие, более сильным взаимодействием между молекулами, а значит большей прочностью кристаллической решётки вещества. Молекулы же нечётного ряда взаимодействуют слабее, соответственно, разрушить их взаимодействие при нагревании проще.
Химические свойства
Таблица основных свойств карбоновых кислот .
| Кислотные свойства | |
| Характерные кислотные свойства проявляются в реакциях с металлами, гидроксидами и основными оксидами, а также при вытеснении кислоты (более слабой) из соли. | 2CH3COOH + Mg ⟶ (CH3COO)2Mg + H2 CH3COOH + koh ⟶ CH3COO К + H2O CH3COOH + NH4OH ⟶ CH3COONH4 + H2O 2CH3COOH + CaO ⟶ (CH3COO)2C a + H2O 2CH3COOH + Na2SiO3 ⟶ H2SiO3 + 2CH3COONa |
| Диссоциация | |
| В водных растворах поведение монокарбоновых аналогично поведению одноосновных: происходит ионизация молекулы с образованием иона водорода и карбоксилат иона. | RCOOH ⟶ RCOO — + Н + |
| Восстановление | |
| Восстановление до спирта происходит при помощи литийалюминийгидрида (LiAlH4), а также при кипячении в тетрагидрофуране. Плюсом восстановления в диборане (B2H4) является то, что процесс идёт в более мягких условиях и восстановление других функциональных групп не происходит (NO2, COOR и СN). | CH3(CH2)4COOH + H2 → CH3(CH2)4CH2OH + H2O |
| Окисление | |
| В атмосфере кислорода происходит окисление с выделением углекислого газа и воды. | CH3COOH + 2O2 ⟶ 2СO2 + 2H2O |
| Декарбоксилирование | |
Насыщенные одноосновные огранические соединения сложно подвергаются декарбоксилированию даже при нагревании из-за прочности связи углерод-углерод:
|
|
| Реакция этерификации | |
| Нагревание в присутствии H2SO4 спирта и карбоновой кислоты приводит к сложным эфирам | CH3COOH + CH3CH2OH ⟶ CH3COOCH2CH3 + H2O |
| Образование производных | |
Замещение гидроксильной группы другой функциональной группой (Х) приводит к образованию веществ с общей формулой RCO — X . Это могут быть, например:
|
|
| Получение ангидридов | |
| Производные общей формулой R-C(O)-O-C(O)-R получают межмолекулярной дегидратацией карбоновых органических соединений. Реакция проходит в присутствии водоотнимающего агента (P2O5). | CH3COOH + CH3COOH ⟶ CH3 -C(O)-O-C(O)- CH3 |
| Галогенирование | |
| Взаимодействие с галогенами на свету приводит к образованию галогензамещённых (α-галогенкарбоновых) кислот. | C2H5COOH + Br2 ⟶ CH3CH(Br)COOH + HBr или CH3COOH + 3Cl2 ⟶ C(Cl)3COOH + 3HCl |
Карбоновые считаются слабыми кислотами . При этом монокарбоновые слабее ди- и трикарбоновых кислот. Заместители, являющиеся донорами электронов, ослабляют кислотные свойства, а электроноакцепторные заместители их усиливают, как и кратные связи. Чем дальше заместитель от карбоксильной группы, тем слабее его влияние.
К важным свойствам таких производных, как соли относится реакция получения кетонов методом пиролиза. Кальциевые, ториевые или бариевые соли при нагревании до температуры около 300 °С превращаются в кетоны.
Способы получения
В лаборатории можно получить:

Промышленные способы синтеза основаны на окислении углеводородов с длинными углеводородными цепями. Процесс многоступенчатый с множеством побочных продуктов.
Окисление алкенов: 2CH3-CH2-CH2-CH3 + 5O2 → 4CH3COOH + 2H2O.
Окисление алкенов: CH2=CH2 + O2 → CH3COOHСH3-CH=CH2 + 4[O] → CH3COOH + HCOOH.
Некоторые кислоты (такие как муравьиная, масляная, уксусная, валериановая и прочие) получаются специфическими способами с использованием природных ингредиентов (жиров, эфирных масел, восков).
Применяют кислоты в химической промышленности в качестве исходных соединений для органического синтеза, например, галогенкислот, кетонов, виниловых эфиров.
Области применения муравьиной кислоты основаны на её бактерицидных свойствах. Она применяется в качестве антисептика, в пищевой промышленности, а так же сельском хозяйстве как консервант.
В пищевой, химической, фармацевтической промышленности, а также в домашнем хозяйстве активно применяется уксусная.
 Масляная кислота в химической промышленности
используется в качестве вещества, из которого производят ароматизаторы, пластификаторы, с её помощью экстрагируют щелочно-земельные металлы.
Масляная кислота в химической промышленности
используется в качестве вещества, из которого производят ароматизаторы, пластификаторы, с её помощью экстрагируют щелочно-земельные металлы.
Щавелевая может применяться в качестве реагента в аналитической химии органических веществ, в металлургической промышленности, для приготовления чернил.
Стеариновая C17H35COOH, пальмитиновая C15H31COOH используются как компонент косметических средств, в качестве смазочного материала при обработке металлов. Их натриевая соль является поверхностно активным веществом.
Альдегидами называют соединения, молекулы которых содержат карбонильную группу, соединенную с атомом водорода, т.е. общая формула альдегидов может быть записана как
где R – углеводородный радикал, который может быть разной степени насыщенности, например, предельный или ароматический.
Группу –СНО называют альдегидной.
Кетоны – органические соединения, в молекулах которых содержится карбонильная группа, соединенная с двумя углеводородными радикалами. Общую формулу кетонов можно записать как:
где R и R’ – углеводородные радикалы, например, предельные (алкилы) или ароматические.
Гидрирование альдегидов и кетонов
Альдегиды и кетоны могут быть восстановлены водородом в присутствии катализаторов и нагревании до первичных и вторичных спиртов соответственно:
Окисление альдегидов
Альдегиды легко могут быть окислены даже такими мягкими окислителями, как гидроксид меди и аммиачный раствор оксида серебра.
При нагревании гидроксида меди с альдегидом происходит исчезновение изначального голубого окрашивания реакционной смеси, при этом образуется кирпично-красный осадок оксида одновалентной меди:
В реакции с аммиачным раствором оксида серебра вместо самой карбоновой кислоты образуется ее аммонийная соль, поскольку находящийся в растворе аммиак реагирует с кислотами:
Кетоны в реакцию с гидроксидом меди (II) и аммиачным раствором оксида серебра не вступают. По этой причине эти реакции являются качественными на альдегиды. Так реакция с аммиачным раствором оксида серебра при правильной методике ее проведения приводит к образованию на внутренней поверхности реакционного сосуда характерного серебряного зеркала.
Очевидно, что если мягкие окислители могут окислить альдегиды, то само собой это могут сделать и более сильные окислители, например, перманганат калия или дихромат калия. При использовании данных окислителей в присутствии кислот образуются карбоновые кислоты:
Химические свойства карбоновых кислот
Карбоновыми кислотами называют производные углеводородов, содержащие одну или несколько карбоксильных групп.
Карбоксильная групп а:
Как можно видеть, карбоксильная группа состоит из карбонильной группы –С(О)- , соединенной с гидроксильной группой –ОН.
В связи с тем, что к гидроксильной группе непосредственно прикреплена карбонильная, обладающая отрицательным индуктивным эффектом связь О-Н является более полярной, чем в спиртах и фенолах. По этой причине карбоновые кислоты обладают заметно более выраженными, чем спирты и фенолы, кислотными свойствами. В водных растворах они проявляют свойства слабых кислот, т.е. обратимо диссоциируют на катионы водорода (Н+) и анионы кислотных остатков:
Реакции образования солей
С образованием солей карбоновые кислоты реагируют с:
1) металлами до водорода в ряду активности:
2) аммиаком
3) основными и амфотерными оксидами:
4) основными и амфотерными гидроксидами металлов:
5) солями более слабых кислот – карбонатами и гидрокарбонатами, сульфидами и гидросульфидами, солями высших (с большим числом атомов углерода в молекуле) кислот:
Систематические и тривиальные названия некоторых кислот и их солей представлены в следующей таблице:
| Формула кислоты | Название кислоты тривиальное/систематическое | Название соли тривиальное/систематическое |
| HCOOH | муравьиная/ метановая | формиат/ метаноат |
| CH 3 COOH | уксусная/ этановая | ацетат/ этаноат |
| CH 3 CH 2 COOH | пропионовая/ пропановая | пропионат/ пропаноат |
| CH 3 CH 2 CH 2 COOH | масляная/ бутановая | бутират/ бутаноат |
Следует помнить и обратное: сильные минеральные кислоты вытесняют карбоновые кислоты из их солей как более слабые:
Реакции с участием ОН группы
Карбоновые кислоты вступают в реакцию этерификации с одноатомными и многоатомными спиртами в присутствии сильных неорганических кислот, при этом образуются сложные эфиры:
Данного типа реакции относятся к обратимым, в связи с чем с целью смещения равновесия в сторону образования сложного эфира их следует осуществлять, отгоняя более летучий сложный эфир при нагревании.
Обратный реакции этерификации процесс называют гидролизом сложного эфира:
Необратимо данная реакция протекает в присутствии щелочей, поскольку образующаяся кислота реагирует с гидроксидом металла с образованием соли:
Реакции замещения атомов водорода в углеводородном заместителе
При проведении реакций карбоновых с хлором или бромом в присутствии красного фосфора при нагревании происходит замещение атомов водорода при α-атоме углерода на атомы галогена:
В случае большей пропорции галоген/кислота может произойти и более глубокое хлорирование:
Реакции разрушения карбоксильной группы (декарбоксилирование)
Особые химические свойства муравьиной кислоты
Молекула муравьиной кислоты, несмотря на свои малые размеры, содержит сразу две функциональные группы:
В связи с этим она проявляет не только свойства кислот, но также и свойства альдегидов:
При действии концентрированной серной кислоты муравьиная кислота разлагается на воду и угарный газ.
Урок поможет вам получить представление о теме «Химические свойства предельных одноосновных карбоновых кислот» (школьная программа по химии 10 класса). В ходе занятия вы узнаете про химические свойства предельных карбоновых кислот, которые обусловлены наличием в их молекуле карбоксиловой группы.
Тема: Карбонильные соединения. Карбоновые кислоты
Урок: Химические свойства предельных одноосновных карбоновых кислот
Из названия этих соединений можно предположить, что им характерны кислотные свойства.
Кислотные свойства
Кислотные свойства - способность к отщеплению иона водорода.
 ⇆ +H +
⇆ +H +
В чем проявляются кислотные свойства карбоновых кислот?
1. Наличие свободного иона водорода в растворах кислот обуславливает их кислый вкус и взаимодействие с индикаторами.

2. Кислоты взаимодействуют с активными металлами, выделяя водород:
2СН 3 СOOH + Mg →(СН 3 СOO) 2 Mg + H 2 .
этанат магния
(ацетат магния)
3. Реакции c основаниями:
СН 3 СOOH + NaOH → СН 3 СOONa + H 2 O.
4. Реакции с основными оксидами:
2СН 3 СOOH + ZnO → (СН 3 СOO) 2 Zn + H 2 O.
5. Реакции с солями более слабых кислот:
Электролит - вещество, диссоциирующее на ионы в растворе или расплаве.
Сильный электролит - электролит, диссоциирующий на ионы полностью.
Слабый электролит - электролит, диссоциирующий на ионы частично.
Карбоновые кислоты → слабые электролиты:
СН 3 СООН СН 3 СОО - + Н +

От чего зависит сила карбоновой кислоты?
1. От строения
Чем больше положительный заряд на атоме водорода в молекуле кислоты, тем более сильным электролитом она будет. Наличие электронодонорных углеводородных радикалов рядом с карбоксильной группой уменьшает способность кислоты диссоциировать.


2. От наличия других групп в молекуле
Введение электроноакцепторных заместителей увеличивает положительный заряд на атоме водорода и силу кислоты.


Нуклеофильное замещение (реакция этерификации)
Карбоновые кислоты взаимодействуют со спиртами в присутствии катализатора - серной кислоты, образуя сложные эфиры .
Декарбоксилирование - удаление карбоксильной группы.
1. При нагревании с твердыми щелочами соли карбоновых кислот дают алкан с числом атомов углерода на единицу меньше, а карбоксильная группа удаляется в виде карбоната:
RCOONa тв + NaOH тв RH + Na 2 CO 3 .
2. Твердые соли карбоновых кислот со щелочноземельными металлами при нагревании дают кетон и карбонат:
(СН 3 СОО) 2 Са СН 3 -СО-СН 3 + СаСО 3 .
3. Бензойная кислота при прокаливании разлагается на бензол и углекислый газ:
Ph-COOH PhH + CO 2 .
4. При электролизе водных растворов солей карбоновых кислот на аноде выделяется углекислый газ, а углеводородные радикалы объединяются в алкан (реакция Кольбе):
2RCOONa + Н 2 О → R-R + 2CO 2 + 2NaOH.
При электролизе без диафрагмы (с неразделенным катодным и анодным пространством) гидроксид натрия взаимодействует с углекислым газом, и одним из продуктов является гидрокарбонат:
2RCOONa + Н 2 О →R-R + 2NaHCO 3 .
Подведение итога урока
При помощи данного урока вы смогли самостоятельно изучить тему «Химические свойства предельных одноосновных карбоновых кислот» (школьная программа по химии 10 класса). В ходе занятия вы узнали химические свойства предельных карбоновых (органических) кислот, которые обусловлены наличием в их молекуле карбоксильной группы.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 10 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2008. - 463 с.
3. Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2010. - 462 с.
4. Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
Домашнее задание
1. №№ 2, 4 (с. 113) Рудзитис Г.Е., Фельдман Ф.Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Какие две кислоты имеют общую молекулярную формулу С 4 Н 8 О 2. Назовите их.
3. Какая из кислот монохлоруксусная или уксусная должна быть сильнее? Почему?
Способы получения . 1 . Окисление альдегидов и первичных спиртов - общий способ получения карбоновых кислот. В качестве окислителей применяются />K М n О 4 и K 2 С r 2 О 7 .
2 Другой общий способ - гидролиз галогензамещенных углеводородов, содержащих, три атома галогена у одного атома углерода. При этом образуются спирты, содержащие группы ОН у одного атома углерода - такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:/>
| ЗNаОН | ||||
| R-CCl 3 | → | R — COOH + Н 2 О | ||
| -3NaCl |
3 . Получение карбоновых кислот из цианидов (нитрилов) - это важный способ, позволяющий наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия, например:/>
СН 3 -В r + NaCN → CH 3 — CN + NaBr .
Образующийся нитрил уксусной кислоты (метилцианид) при нагревании легко гидролизуется с образованием ацетата аммония:
CH 3 CN + 2Н 2 О → CH 3 COONH 4 .
При подкислении раствора выделяется кислота:
CH 3 COONH 4 + HCl → СН 3 СООН + NH 4 Cl .
4 . Использование реактива Гриньяра по схеме:/>
Н 2 О
R
—
MgBr
+ СО 2 →
R
—
COO
—
MgBr
→
R
—
COOH
+
Mg
(OH
)
Br
5 . Гидролиз сложных эфиров:/>
R — COOR 1 + КОН → R — COOK + R ‘ OH ,
R — COOK + HCl → R — COOH + KCl .
6 . Гидролиз ангидридов кислот:/>
(RCO ) 2 O + Н 2 О → 2 RCOOH .
7 . Для отдельных кислот существуют специфические способы получения./>
Муравьиную кислоту получают нагреванием оксида углерода (II ) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
Уксусную кислоту получают каталитическим окислением бутана кислородом воздуха:
2С 4 Н 10 + 5 O 2 → 4СН 3 СООН + 2Н 2 О.
Для получения бензойной кислоты можно использовать окисление монозамешенных гомологов бензола кислым раствором перманганата калия:
5С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 = 5С 6 Н 5 СООН + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O .
Кроме того, бензойную кислоту можно получить из бензальдегида с помощью реакции Канниццаро . В этой реакции бензальдегид обрабатывают 40-60%-ным раствором гидроксида натрия при комнатной температуре. Одновременное окисление и восстановление приводит к образованию бензойной кислоты и соответственно фенилметанола (бензилового спирта):
Химические свойства . Карбоновые кислоты - более сильные кислоты, чем спирты, поскольку атом водорода в карбоксильной группе обладает повышенной подвижностью благодаря влиянию группы СО. В водном растворе карбоновые кислоты диссоциируют:/>
RCOOH
![]() RCOO — + Н +
RCOO — + Н +
Тем не менее из-за ковалентного характера молекул карбоновых кислот указанное выше равновесие диссоциации достаточно сильно сдвинуто влево. Таким образом, карбоновые кислоты - это, как правило, слабые кислоты. Например, этановая (уксусная) кислота характеризуется константой диссоциации К а = 1,7*10 -5 . />
Заместители, присутствующие в молекуле карбоновой кислоты, сильно влияют на ее кислотность вследствие оказываемого ими индуктивного эффекта . Такие заместители, как хлор или фенильный радикал оттягивают на себя электронную плотность и, следовательно, вызывают отрицательный индуктивный эффект (-/). Оттягивание электронной плотности от карбоксильного атома водорода приводит к повышению кислотности карбоновой кислоты. В отличие от этого такие заместители, как алкильные группы, обладают электронодонорными свойствами и создают положительный индуктивный эффект, +I. Они понижают кислотность. Влияние заместителей на кислотность карбоновых кислот наглядно проявляется в значениях констант диссоциации K a для ряда кислот. Кроме того, на силу кислоты оказывает влияние наличие сопряженной кратной связи.
|
Карбоновые кислоты Формула K a |
|
Пропионовая CH 3 CH 2 COOH 1,3*10 -5 |
|
Масляная CH 3 CH 2 CH 2 COOH 1,5*10 -5 |
|
Уксусная CH 3 COOH 1,7*10 -5 |
|
Кротоновая CH 3 — CH = CH — COOH 2,0*10 -5 |
|
Винилуксусная CH 2 =CH-CH 2 COOH 3,8*10 -5 |
|
Акриловая CH 2 =CH-COOH 5,6*10 -5 |
|
Муравьиная HCOOH 6,1*10 -4 |
|
Бензойная C 6 H 5 COOH 1,4*10 -4 |
|
Хлоруксусная CH 2 ClCOOH 2,2*10 -3 |
|
Тетроновая CH 3 — C ≡ C — COOH 1,3*10 -3 |
|
Дихлоруксусная CHCl 2 COOH 5,6*10 -2 |
|
Щавелевая HOOC — COOH 5,9*10 -2 |
|
Трихлоруксусная CCl 3 COOH 2,2*10 -1 |
Взаимное влияние атомов в молекулах дикарбоновых кислот приводит к тому, что они являются более сильными, чем одноосновные.
2. Образование солей. Карбоновые кислоты обладают всеми свойствами обычных кислот. Они реагируют с активными металлами, основными оксидами, основаниями и солями слабых кислот:
2 RCOOH + М g → (RCOO ) 2 Mg + Н 2 ,
2 RCOOH + СаО → (RCOO ) 2 Ca + Н 2 О,
RCOOH + NaOH → RCOONa + Н 2 О,
RCOOH + NaHCO 3 → RCOONa + Н 2 О + СО 2 .
Карбоновые кислоты - слабые, поэтому сильные минеральные кислоты вытесняют их из соответствующих солей:
CH 3 COONa + HCl → СН 3 СООН + NaCl .
Соли карбоновых кислот в водных растворах гидролизованы:
СН 3 СООК + Н 2 О
![]() СН 3 СООН + КОН.
СН 3 СООН + КОН.
Отличие карбоновых кислот от минеральных заключается в возможности образования ряда функциональных производных.
3 . Образование функциональных производных карбоновых кислот. При замещении группы ОН в карбоновых кислотах различными группами (/>X ) образуются функциональные производные кислот, имеющие общую формулу R -СО- X ; здесь R означает алкильную либо арильную группу. Хотя нитрилы имеют другую общую формулу (R - CN ), обычно их также рассматривают как производные карбоновых кислот, поскольку они могут быть получены из этих кислот.
Хлорангидриды получают действием хлорида фосфора (V ) на кислоты:
R-CO-OH + РС l 5 → R-CO-Cl + РОС l 3 + HCl .
|
Соединение примеры |
|
Кислота
Этановая(уксусная) Бензойная кислота хлорангидрит кислоты
Этаноилхлорид Бензоилхлорид (ацетилхлорид) ангидрид кислоты
Этановый(уксусный) бензойный ангидрит Ангидрит сложый эфир
Этилэтаноат(этилацетат) Метилбензоат амид Этанамид(ацетамид) Бензамид Нитрил Этаннитрил Бензонитрил (ацетонитрил) |
Ангидриды образуются из карбоновых кислот при действии водоотнимающих средств:
2 R — CO — OH + Р 2 О 5 → (R — CO -) 2 O + 2НРО 3 .
Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты (обратимая реакция этерификации):
Механизм реакции этерификации был установлен методом "меченых атомов".
Сложные эфиры можно также получить при взаимодействии хлорангидридов кислот и алкоголятов щелочных металлов:
R-CO-Cl + Na-O-R’ → R-CO-OR’ + NaCl .
Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов :
СН 3 -СО-С l + CН 3 → СН 3 -СО-CН 2 + HCl .
Кроме того, амиды могут быть получены при нагревании аммонийных солей карбоновых кислот:
При нагревании амидов в присутствии водоотнимающих средств они дегидратируются с образованием нитрилов :
| Р 2 0 5 | ||
| CH 3 — CO — NH 2 |
→ |
CH 3 — C ≡ N + Н 2 О |
Функциональные производные низших кислот — летучие жидкости. Все они легко гидролизуются с образованием исходной кислоты:
R-CO-X + Н 2 О →R-CO-OH + НХ .
В кислой среде эти реакции могут быть обратимы. Гидролиз в щелочной среде необратим и приводит к образованию солей карбоновых кислот, например:
R-CO-OR ‘ + NaOH → R-CO-ONa + R’OH.
4 . Ряд свойств карбоновых кислот обусловлен наличием углеводородного радикала. Так, при действии галогенов на кислоты в присутствии красного фосфора образуются галогензамещенные кислоты, причем на галоген замещается атом водорода при соседнем с карбоксильной группой атоме углерода (а-атоме):/>
| р кр | ||
|
СН 3 -СН 2 -СООН + Вr 2 |
→ |
СН 3 -СНВr-СООН + НВr |
Непредельные карбоновые кислоты способны к реакциям присоединения:
СН 2 =СН-СООН + Н 2 → СН 3 -СН 2 -СООН,
СН 2 =СН-СООН + С l 2 → СН 2 С l -СНС l -СООН,
СН 2 =СН-СООН + HCl → СН 2 С l -СН 2 -СООН,
СН 2 =СН-СООН + Н 2 O → НО-СН 2 -СН 2 -СООН,
Две последние реакции протекают против правила Марковникова.
Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации .

5 . Окислительно-восстановительные реакции карбоновых кислот./>
Карбоновые кислоты при действии восстановителей в присутствии катализаторов способны превращаться в альдегиды, спирты и даже углеводороды:
Муравьиная кислота НСООН отличается рядом особенностей, поскольку в ее составе есть альдегидная группа:
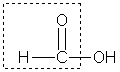
Муравьиная кислота - сильный восстановитель и легко окисляется до СО 2 . Она дает реакцию "серебряного зеркала" :
НСООН + 2OH → 2Ag + (NH 4) 2 CO 3 + 2NH 3 + H 2 O,
или в упрощенном виде:
C Н 3 НСООН + Аg 2 О → 2Аg + СО 2 + Н 2 О.
Кроме того, муравьиная кислота окисляется хлором:
НСООН + Сl 2 → СО 2 + 2 HCl .
В атмосфере кислорода карбоновые кислоты окисляются до СО 2 и Н 2 О:
СН 3 СООН + 2О 2 → 2СО 2 + 2Н 2 О.
6 . Реакции декарбоксширования . Насыщенные незамещенные монокарбоновые кислоты из-за большой прочности связи С-С при нагревании декарбоксилируются с трудом. Для этого необходимо сплавление соли щелочного металла карбоновой кислоты со щелочью:/>
Появление электронодонорных заместителей в углеводородном радикале способствует реакции декарбоксилирования :
Двухосновные карбоновые кислоты легко отщепляют СО 2 при нагревании: